Углеводороды и их свойства-это база органической химии, потому как все остальные молекулы, обладающие органической природой, рассматриваются именно как производные углеводородов. Одним из важнейших функциональных производных углеводородов являются кислородсодержащие органические соединения, рассмотрение которых следует начать с изучения темы “спирты”.
Спирты это функциональные производные углеводородов, которые в составе имеют одну или несколько гидроксильных групп (ОН— ), в свою очередь связанных с насыщенным атомом углерода, то есть находящимся в sp 3 гибридном состоянии.
Общая формула: R-OH
R-предельный радикал. Например: CH3 -метил, C2H5-этил, C3H7-пропил
Строение спиртов
В молекулах спиртов фигурируют такие ковалентно-неполярные С–С и ковалентно-полярные С–Н, О–Н и С–О химические связи

Так как кислород находится в периодической таблице Д.И. Менделеева правее атома углерода, то его электроотрицательность (ЭО = 3,5) больше электроотрицательности углерода (ЭО = 2,4), и тем более водорода (ЭО = 2,1), поэтому электронная плотность связей С-О и С-Н смещена к более электроотрицательному атому кислорода.
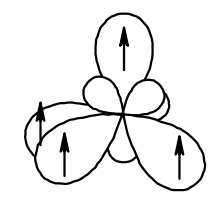
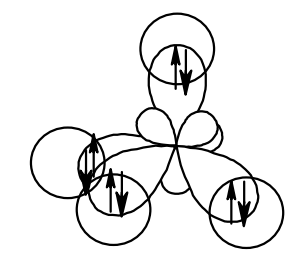
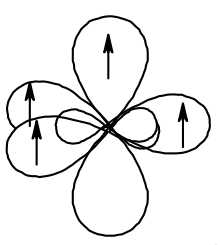
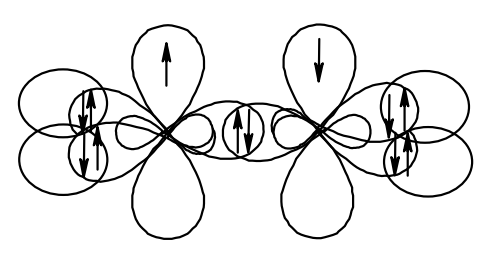
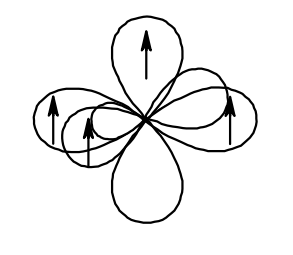
Атом кислорода в спиртах находится в состоянии sp3-гибридизации. В образовании химических связей с атомами C и H участвуют две 2sp3-гибридные орбитали, а еще две 2sp3-гибридные орбитали заняты неподеленными электронными парами атома кислорода. Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108о.

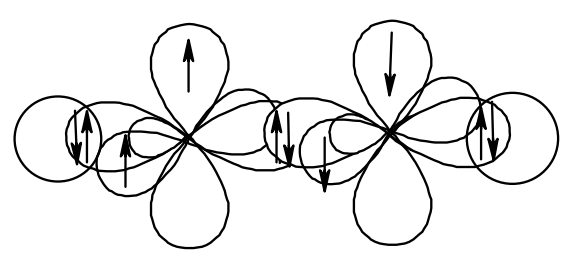
Спирты, как и множество других органических соединений , характеризуются наличием водородной связи между молекулами. Так, атом водорода одной молекулы, связанный с сильно электроотрицательным атомом(F, Cl, N,O), в нашем случае с атомом кислорода, способен взаимодействовать с неподеленной парой электронов атома кислорода другой молекулы, с образованием дополнительной слабой связи-водородной. Таким образом, в молекулах спиртов за счет межмолекулярных водородных связей образуются ассоциаты. Водородная связь влияет на физические свойства спиртов.
Номенклатура и изомерия спиртов
Для названия спиртов используют используют систематическую, радикально-функциональную и тривиальную номенклатуру. Подробнее об этом можно ознакомившись со статьей.
Структурная изомерия
Такие оксосодержащие соединения как спирты способны образовывать изомеры, то есть изомеризоваться. Так, для спиртов присуща изомерия углеродного скелета, изомерия положения гидроксильной группы и межклассовая изомерия.
Структурные изомеры — это соединения, имеющие одинаковый химический состав, но отличающиеся строением молекул.
Спирты состоящие из четырех и более атомов углерода отличаются наличием изомерии углеродного скелета. Например. Формуле С4Н8ОН соответствуют четыре структурных изомера, из них два различаются строением углеродного скелета

Изомерия функциональной группы характеризуется изменением положения гидроксигруппы в молекуле спирта. Данная изомерия характерна для спиртов, которые содержат три или более атомов углерода.
Например, пропанол-1 и пропанол-2

Межклассовые изомеры — это вещества, относящиеся к разным классам органических веществ, обладающие различным строением, но имеющие одинаковый состав. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
Например, межклассовые изомеры с общей формулой С3Н7ОH: пропиловый спирт СН3–CH2-CH2–OH и метилэтиловый эфир CH3–O–CH2-CH3
Получение спиртов
1. Щелочной гидролиз галогенпроизводных углеводородов
Этот метод-один из самых распространенных лабораторных способов получения спиртов. В ходе реакции алкилгалогенид взаимодействует с водным раствором щелочи и атом галогена заменяется на гидроксогруппу. Легче всего реакцию гидролиза вступают третичные галогенпроизводные углеводороды, труднее-первичные.
2. Гидратация алкенов
В промышленности этиловый, изопропиловый и трет-бутиловый спирт получают путем гидратации алкенов. Эта реакция протекает с использованием кислотных катализаторов. Следует помнить, что присоединение воды к несимметричным алкенам протекает по правилу Марковникова(см. алкены)
3. Восстановление карбонильных соединений
В ходе каталитического гидрирования альдегидов образуются первичные спирты, а при гидрировании кетонов — вторичные спирты, а из формальдегида образуется метанол. Реакция протекает при повышенной температуре, а в качестве катализатора используют платину
Например, при гидрировании этаналя образуется этанол
Например: при гидрировании ацетона образуется изопропанол
Например, гидрирование диальдегида – один из способов получения этиленгликоля
4. Окисление алкенов холодным водным раствором перманганата калия
Алкены реагируют с водным раствором перманганата калия без нагревания. При этом образуются двухатомные спирты (гликоли).
5. Промышленное получение метанола из «синтез-газа»
До открытия этого метода метанол получали сухой перегонкой древесины-нагреванием без доступа воздуха. В настоящее время метанол получают из “синтез-газа”- каталитический синтез метанола из монооксида углерода и водорода при 300-400°С и давления 500 атм в присутствии смеси оксидов цинка, меди хрома.
CO + 2H2 ⇄ CH3OH
6. Получение этанола ферментативным брожением сахаров (спиртовое брожение)
Для глюкозы характерно ферментативное брожение, то есть распад молекул на части под действием ферментов. Один из вариантов — спиртовое брожение.
7. Гидролиз жиров – способ получения многоатомных спиртов
Под действием кислоты жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
Например: при гидролизе тристеарата глицерина образуется глицерин и стеариновая кислота
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
Например: при щелочном гидролизе тристеарата глицерина образуется глицерин и соль стеариновой кислоты (стеарат)
Физические свойства спиртов
Спирты, содержащие не более 11 атомов углерода являются жидкими веществами. Более высшие гомологи находятся в твердом агрегатном состоянии.
Спирты состава С1-С3 имеют характерный алкогольный запах и жгучий вкус, смешиваются с водой в любых соотношениях.
Плотность спиртов меньше единицы, то есть они легче воды
Спирты имеют более высокую температуру кипения и большую растворимость в воде по сравнению с соответствующими углеводородами и галогенуглеводородами по причиние наличия водородной связи между кислородом одной молекулы спирта и водородом другой молекулы.
С увеличением длины углеводородной цепи спиртов их температура кипения повышается, а растворимость уменьшается.
По мере увеличения разветвления углеродного скелета площадь поверхности молекулы уменьшается, что, в свою очередь, уменьшает силу притяжения молекул, то есть Ван-дер-Ваальсово взаимодействие молекул, и, следовательно, снижает температуру кипения. Таким образом, температура кипения разветвленных изомеров ниже, чем у соответствующих прямо цепочечных изомеров
Вода и спирты обладают схожими свойствами в связи с наличием гидроксильных групп в молекулах воды. Эти группы способны формировать водородные связи как с другими молекулами воды, так и с молекулами спирта. Аналогично, молекулы спирта могут образовывать водородные связи как с другими молекулами спирта, так и с водой. Именно благодаря образованию водородных связей со водой, спирты, как правило, обладают сильной растворимостью в воде. Гидроксильная группа, которая обеспечивает такую растворимость, называется гидрофильной, поскольку она способна образовывать водородные связи с водой и повышать растворимость спирта в ней. Метанол, этанол, n-пропиловый спирт, изопропиловый спирт, трет-бутиловый спирт — все они могут смешиваться с водой. Однако, спирты с большей молекулярной массой, обычно, менее растворимы в воде, поскольку их углеводородная часть, которая обладает гидрофобностью, увеличивается с ростом молекулярной массы. Благодаря своей сильной полярности, спирты являются лучшими растворителями для ионных соединений и других полярных веществ по сравнению с соответствующими углеводородами.
Химические свойства спиртов
Спирты обладают разнообразной реакционной способностью. Эта характеристика обусловлена строением этих соединений. В молекуле спиртов можно выделить такие реакционные центры, как ОН группа. Она является кислотным центром, то есть воспринимает атаку основаниями и в результате происходит отщепление протона. Нуклеофильный и основный центр-атом кислорода, который имеет неподеленную пару электронов, благодаря которому спирты могут выступать как нуклеофильные реагенты. Также можно выделить, электрофильный центр-атом углерода, который связан с более электроотрицательным атомом кислорода гидроксогруппы, что является причиной имеющегося дефицита электронов на данном атоме углерода. И он, в свою очередь, способен взаимодействовать с нуклеофильными реагентами
Рассмотрим подробнее распределение зарядов на атомах в молекуле спирта. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–. Разрыв таких связей протекает по по ионному механизму. Разрыв связи О–Н с отрывом иона Н+ соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения. Реакции окисления характеризуются разрывом связи О–Н, а процесс восстановления протекает с разрывом С–О связи
Как итог, химические свойства спиртов можно представить следующим образом:
- слабые кислотные свойства, замещение водорода на металл;
- замещение группы ОН
- элиминирование – дегидратация, то есть отрыв воды
- окисление
- образование сложных эфиров — этерификация
1. Кислотные свойства
Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды.
1.1. Взаимодействие с раствором щелочей
При взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты-бесцветные твердые вещества растворяются в спиртах и почти полностью гидролизуются водой. Поэтому равновесие реакции сильно смещается в сторону исходных веществ.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому спирты не взаимодействуют с растворами щелочей. Многоатомные спирты, в свою очередь, обладающие несколькими гидроксогруппами являются более сильными кислотами, чем одноатомные спирты. Поэтому способны к более выраженному взаимодействию с щелочами.
1.2. Взаимодействие с металлами (щелочными)
Спирты взаимодействуют с щелочными металлами с образованием алкоголятов(этоксидов). Реакция взаимодействия спиртов с активными металлами протекает подобно реакции взаимодействия этих металлов с кислотами, то есть с выделением водорода.
Например, этанол взаимодействует с калием с образованием этилата калия и водорода.
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
Например, этилат калия разлагается водой:
Многоатомные спирты также реагируют с активными металлами:
Кислотные свойства одноатомных спиртов увеличиваются в ряду:
CH3OH > первичные спирты > вторичные спирты > третичные спирты
Этот ряд объясняется уменьшением эффекта сольватации, который чем больше, тем более выражена кислотная составляющая спиртов. Так, метанол сольватирован сильнее, чем третичный спирт, поскольку метанол стерически более доступен для электростатического взаимодействия с водой, а третичный спирт, характеризующийся большим количеством углеводородных радикалов имеют меньшую способность к сольватации.
1.3. Взаимодействие с гидроксидом меди (II)
Многоатомные спирты взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соли).Данная реакция является аналитически важной, поскольку является качественной на многоатомные спирты.
Например, при взаимодействии этиленгликоля со свежеосажденным гидроксидом меди (II) образуется ярко-синий раствор гликолята меди:
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан. Например, этанол реагирует с хлороводородом с образованием хлорэтана. Или с бромоводородом, образуя бромэтан:
Реакционная способность одноатомных спиртов в реакциях с галогеноводородами уменьшается в ряду:
третичные > вторичные > первичные > CH3OH.
Также для замены гидроксигруппы на галоген можно провести реакцию с тионилхлоридом:
Или с хлоридом фосфора(5):
Многоатомные спирты также, как и одноатомные спирты, реагируют с галогеноводородами.
Например, этиленгликоль реагирует с бромоводородом:
2.2. Взаимодействие с аммиаком
Также реакцию замещения гидроксигруппы на аминогруппу можно провезти при нагревании спирта с аммиаком на катализаторе.
Например, при взаимодействии этанола с аммиаком образуется этиламин.
2.3. Этерификация (образование сложных эфиров)
Одноатомные и многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты):
Многоатомные спирты вступают в реакции этерификации с органическими и неорганическими кислотами.
Например, этиленгликоль реагирует с уксусной кислотой с образованием ацетата этиленгликоля:
Глицерин, он же пропантриол-1,2,3, также вступает в реакцию этерификации. Продуктом этерификации является триацетилглицерин.
2.4. Взаимодействие с кислотами-гидроксидами
Спирты способны вступать в реакцию и с неорганическими кислотами, например, азотной или серной.
Например, при взаимодействии этанола с азотной кислотой образуется сложный эфир этилнитрат:
Например, глицерин под действием азотной кислоты образует тринитрат глицерина
(тринитроглицерин):
3. Реакции отщепления группы ОН
При нагревании спиртов в присутствии минеральных кислот, спирты терпят отщепление воды, то есть происходит дегидратация. В зависимости от условий возможна внутримолекулярная дегидратация и межмолекулярная дегидратация. В результате первой образуется алкен, а в результате второй-простой эфир.
3.1. Внутримолекулярная дегидратация
При высокой температуре (более 140оС) происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
Например, из этанола под действием концентрированной серной кислоты при температуре выше 140 градусов образуется этилен:
В качестве катализатора этой реакции также используют оксид алюминия.
Отщепление воды от несимметричных спиртов проходит в соответствии с эмпирическим правилом Зайцева: водород предпочтительнее отщепляется от менее гидрогенизированного атома углерода. Иначе говоря, образование двойной связи происходит у наиболее замещенного атома углерода.
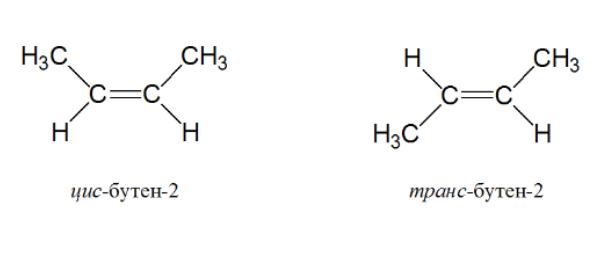
Например, в присутствии концентрированной серной кислоты при нагревании выше 140оС из бутанола-2 в основном образуется бутен-2:
Если этанол пропускать через смесь катализаторов оксид цинка и алюминия при нагревании, то происходит формирование сопряженного диена, а именно бутадиена-1,3. Это реакция носит важный промышленный характер и получила название-синтез Лебедева.
Также алкадиены могут быть получены путем внутримолекулярной дегидратации диолов. Так, в процессе дегидратации бутандиола-1,2 образуется бутадиен-1,3. В роли катализатора кроме серной кислоты, может выступать и оксид алюминия
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140оС) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
Например, при дегидратации этанола при температуре до 140оС образуется диэтиловый эфир:
4. Окисление спиртов
Реакции окисления в органической химии характеризуются введением в молекулу соединения более электроотрицательного атома, чем углерод и/или отщеплением водорода. В зависимости от интенсивности и условий реакции окисление можно представить как каталитическое, мягкое и жесткое.
Каталитическое окисление-применение катализаторов в окислении обеспечивает введение кислорода в органические и неорганические соединения. В отличие от этого, мягкое окисление альтернативно осуществляется без интенсивного нагревания в нейтральной или слабощелочной среде. Нейтральные условия и повышенная температура, а также возможное дополнительное введение кислоты или щелочи отличают жесткие процессы окисления.
При окислении первичных спиртов они последовательно превращаются сначала в альдегиды, а потом в карбоновые кислоты. Глубина окисления зависит от окислителя. Окисление альдегида в карбоновую кислоту можно избежать удалив его из реакционной смеси. Метанол окисляется в формальдегид, который окисляется в муравьиную кислоту. Муравьиная кислота в свою очередь при окислении может превратиться в угольную кислоту. А угольная кислота, характеризующаяся неустойчивостью, распадается на углекислый газ и воду. Вторичные спирты окисляются в кетоны.
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора, оксид марганца(4), катализатор в виде соединений меди, оксида хрома, оксида цинка при нагревании
Легкость окисления спиртов уменьшается в ряду:
метанол < первичные спирты < вторичные спирты < третичные спирты
Продукты окисления многоатомных спиртов зависят от их строения. При окислении оксидом меди многоатомные спирты образуют карбонильные соединения.
4.1. Окисление оксидом меди (II)
Спирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
Например, этанол окисляется оксидом меди до уксусного альдегида
Например, пропанол-2 окисляется оксидом меди (II) при нагревании до ацетона
Третичные спирты окисляются только в жестких условиях, благодаря чему их можно отличить от первичных и вторичных спиртов по реакции с разбавленным щелочным раствором перманганата калия.
4.2. Окисление кислородом в присутствии катализатора
Спирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.). Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
Например, при окислении пропанола-1 образуется пропаналь
Например, пропанол-2 окисляется кислородом при нагревании в присутствии меди до ацетона
Третичные спирты окисляются только в жестких условиях.
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) первичные спирты окисляются до карбоновых кислот, вторичные спирты окисляются до кетонов, метанол окисляется до углекислого газа.
При нагревании первичного спирта с перманганатом или дихроматом калия в кислой среде может образоваться также альдегид, если его сразу удаляют из реакционной смеси.
Третичные спирты окисляются только в жестких условиях (в кислой среде при высокой температуре) под действием сильных окислителей: перманганатов или дихроматов. При этом происходит разрыв углеродной цепи и могут образоваться углекислый газ, карбоновая кислота или кетон, в зависимости от строения спирта.
Например, при взаимодействии метанола с перманганатом калия в серной кислоте образуется углекислый газ
Например, при взаимодействии этанола с перманганатом калия в серной кислоте образуется уксусная кислота
Например, при взаимодействии изопропанола с перманганатом калия в серной кислоте образуется ацетон
Многоатомные спирты окисляются в жестких условиях до углекислого газа. Например, окисляя этиленгликоль в перманганатом калия в кислой среде получим углекислый газ
Деструктивное окисление глицерина происходит подобным образом:
4.4. Горение спиртов
Спирты горят, как и большинство органических соединений(не содержащих каких либо гетероатомов). Так, образуются углекислый газ и вода и выделяется большое количество теплоты.
CnH2n+1ОН + 3n/2O2 → nCO2 + (n+1)H2O + Q
Например, уравнение сгорания метанола:
2CH3OH + 3O2 = 2CO2 + 4H2O
5. Дегидрирование спиртов
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования, то есть происходит отщепление водорода от кислорода, которые свою очередь, обладая избытком электронной плотности, способен образовать еще одну связь с атомом углерода, имеющим частично положительный заряд. Таким образом, при дегидрировании можем наблюдать формирование карбонильной группы. При дегидрировании метанола и первичных спиртов образуются альдегиды, при дегидрировании вторичных спиртов образуются кетоны.
Например, при дегидрировании этанола образуется этаналь
Например, при дегидрировании этиленгликоля образуется диальдегид (глиоксаль)
Применение
Спирты, такие как этанол (этиловый спирт) и изопропиловый спирт, играют важную роль в медицине, промышленности, науке и повседневной жизни. Давайте рассмотрим некоторые из основных областей их применения.
1.Медицинское применение:
Спирты широко используются в медицинских целях в качестве антисептиков и дезинфицирующих средств. Изопропиловый спирт и этанол часто используются для обработки кожи перед инъекциями, а также для дезинфекции поверхностей и медицинского оборудования.
2.Промышленное применение:
В промышленности спирты являются важными растворителями и используются в производстве лакокрасочных материалов, клеев, масел и других химических продуктов. Этанол также используется в производстве косметики и парфюмерии.
3.Энергетическое применение:
Спирты могут служить как альтернативное топливо. Этанол, получаемый из биомассы, используется в биотопливе, что способствует снижению зависимости от нефти и уменьшению выбросов углерода.
4. Лабораторные исследования:
В лабораторной практике спирты широко применяются в качестве растворителей для химических веществ. Они также используются для промывки и дезинфекции лабораторного оборудования.
5.Повседневное использование:
Спирты часто используются в быту для обработки ран, очистки поверхностей и приготовления медицинских средств, таких как настойки и тинктуры.
Заключение:
Спирты-важные органические соединения, изучение свойств, которых закладывает необходимый для понимании процессов и закономерностей органической химии.
Спирты играют важную и незаменимую роль в различных сферах нашей жизни. Их применение охватывает медицину, промышленность, энергетику, науку и быт. Важно обеспечивать безопасное и разумное использование этих веществ, с учетом их полезных свойств и потенциальных рисков.































































































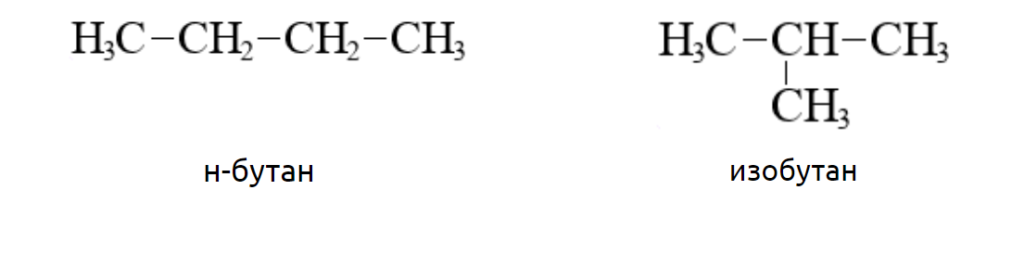
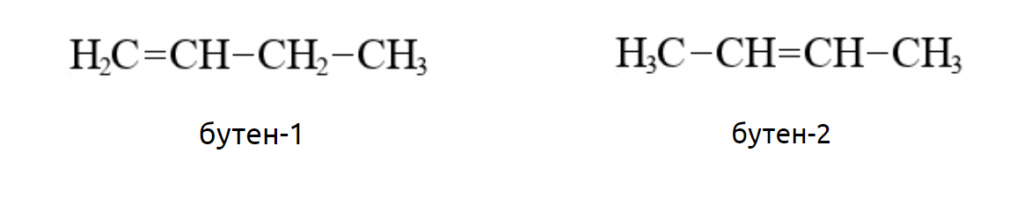
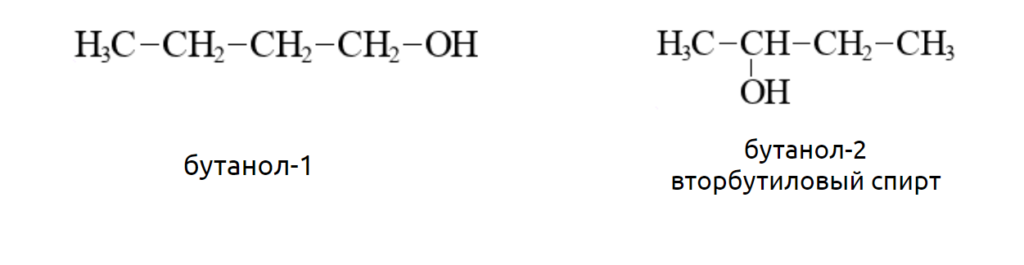
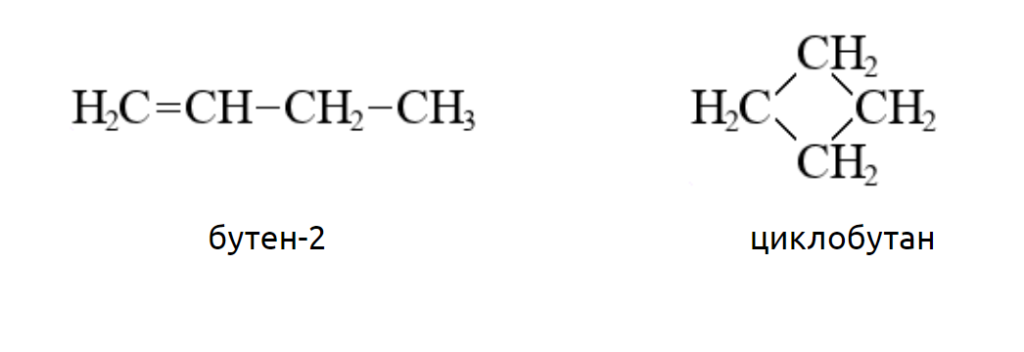































Новости
22.11.2024
22.11.2024
24.10.2024
14.10.2024
09.10.2024
01.10.2024